Em 2018 o Ministério da Saúde atualizou o Protocolo Clínico e Diretrizes Terapêuticas para Hepatite C e Coinfecções que revê e atualiza o que foi publicado em 2015.
Este artigo abordará especificamente as indicações e contra-indicações segundo este protocolo. O conteúdo apresentado será um extrato do protocolo do Ministério da Saúde, posto que não há a intenção de substituí-lo em consultas mais detalhadas e específicas.
Para uma leitura mais completa sobre hepatite C e linhas mais abrangentes do tratamento recomendamos os textos HEPATITE C: Diagnóstico, Evolução e Tratamento – parte I e HEPATITE C: Diagnóstico, Evolução e Tratamento – parte II.
Protocolo Clínico e Diretrizes Terapêuticas para Hepatite C 2018
Esta versão do protocolo apresenta, entre as principais inovações, a ampliação do acesso ao tratamento para todos os pacientes portadores de hepatite C, independentemente, do grau de comprometimento hepático.
O protocolo também inclui o retratamento, para os pacientes que não obtiveram a resposta virológica sustentada em tratamentos anteriores.
Um inovação desta publicação é possibilidade de tratamento dos casos de hepatite C aguda com os antivirais de ação direta.
O vírus da hepatite C (HCV) e suas variantes – Genótipos
Vírus HCV
O vírus da hepatite C possui variações chamadas de genótipos.
Existem, pelo menos, 7 genótipos e 67 subtipos do vírus da hepatite em todo o mundo, porém os três tipos mais comuns no Brasil são os genótipos: os tipos 1, 3 e o 2, nesta ordem.
Os genótipos apresentam respostas distintas aos diferentes tratamentos, por isso, antes é importante saber o genótipo do HVC.
Quando é necessário tratar a hepatite C?
O tratamento da hepatite C está indicado na presença da infecção aguda ou crônica pelo HCV, independentemente do estadiamento da fibrose hepática causada pela infecção
Para começar o tratamento e saber quais medicamentos utilizar, além de conhecer o genótipo do vírus, é necessário avaliar o dano no fígado através da Classificação METAVIR.
A Classificação METAVIR define o o grau de dano no fígado, ou seja, se ainda não há dano ou até se há fibrose avançada (F3) ou cirrose (F4).
Esse diagnóstico poderá afetar a condução clínica do paciente e o esquema de tratamento proposto.
O estadiamento poderá ser realizado por qualquer um dos métodos disponíveis: APRI ou FIB4, biópsia hepática, elastografia hepática. Mais detalhes sobre estes métodos, veja o Protocolo clínico e diretrizes terapêuticas para hepatite viral C e coinfecções.
Classificação METAVIR
Através da biópsia do fígado, retira-se um fragmento de tecido hepático para poder determinar o grau de dano hepático presente.
As mudanças típicas vistas são linfócitos dentro do parênquima, folículos linfóides na tríade portal, alterações dos ductos biliares e fibrose.
A fibrose provocada por hepatite C pode atingir do grau 0 ao 4 (cirrose), conforme a classificação METAVIR:
- F0 = tem fígado normal;
- F1 = alargamento por fibrose restrito ao espaço porta (fibrose discreta);
- F2 = fibrose em espaço porta e com septos incompletos no parênquima hepático (fibrose clinicamente significante);
- F3 = fibrose com septos completos e esboço de nódulos (fibrose avançada);
- F4 = formação de nódulos completos, com distorção significativa da morfologia do parênquima hepático, caracterizando cirrose).
Objetivos do tratamento
O objetivo principal do tratamento é a cura, a erradicação do vírus.
Conseguir a cura significa aumentar a expectativa e a qualidade de vida do paciente, evitando a progressão da infecção para a cirrose, o carcinoma hepatocelular e o óbito.
Com o vírus HCV erradicado do corpo do paciente, pode-se diminuir a incidência de complicações da doença hepática crônica e reduzir a transmissão do HCV.
A erradicação do vírus por meio do tratamento é constatada com o resultado de HCV-RNA indetectável na 12ª ou 24ª semana de seguimento pós-tratamento. Essa condição caracteriza a Resposta Virológica Sustentada (RVS).
Nos pacientes já com cirrose hepática, a erradicação do HCV não remove o risco de hepatocarcinoma ou descompensação clínica.
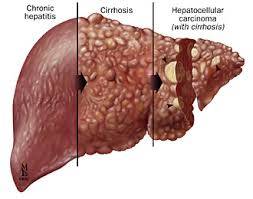
Hepatite C, cirrose e câncer
Indicações de tratamento
A terapia será indicada em todos os pacientes com hepatite C aguda ou crônica, independentemente do estágio da doença.
Na vigência de carcinoma hepatocelular, o tratamento da hepatite C com esquemas livres de interferon é assunto controverso na literatura, considerando a possibilidade de recidiva do tumor após o tratamento.
Entretanto, nesses casos, a indicação ou contraindicação do tratamento deverá ser individualizada.
Em pacientes com perspectiva de transplante em curto prazo (<6 meses), o tratamento deverá ser postergado para o pós-transplante.
Contra-indicações ao tratamento
O tratamento da hepatite C durante a gravidez está contraindicado devido aos efeitos teratogênicos da ribavirina e do alfa-interferon peguilado, isto é: risco de causar malformação fetal, e à ausência de estudos que garantam a segurança dos novos medicamentos antivirais.
A gestação deve ser evitada durante e até 24 semanas após a conclusão do tratamento, para ambos os sexos.
Além da gestação, nem todos as pessoas podem fazer qualquer tipo de medicamento.
Contraindicações ao tratamento com alfa-interferon peguilado
- cardiopatia grave;
- disfunção tireoidiana não controlada;
- distúrbios psiquiátricos não tratados;
- neoplasia recente;
- insuficiência hepática;
- antecedente de transplante que não de fígado;
- distúrbios hematológicos: anemia, leucopenia, plaquetopenia;
- doença autoimune.
Contraindicações ao uso de ribavirina
- Alergia/hipersensibilidade à ribavirina,
- Gravidez: o tratamento apenas deve ser iniciado imediatamente após a obtenção do resultado negativo do teste de gravidez. A gravidez deverá ser evitada por até seis meses após o término do tratamento, pois o medicamento tem ação teratogênica. Essa orientação também vale para os parceiros sexuais das mulheres que desejam engravidar;
- Amamentação;
- História prévia de insuficiência cardíaca grave, incluindo doença cardíaca instável ou não controlada nos seis meses anteriores (a critério médico);
- Disfunção hepática grave ou cirrose descompensada (a critério médico);
- Hemoglobinopatias, como talassemia e anemia falciforme, dentre outras (a critério médico);
- Hemoglobina <8,5g/dL.
Contra-indicações ao tratamento com os antivirais de ação direta (sofosbuvir, simeprevir, daclatasvir)
- arritmia cardíaca: não há dados na literatura que garantam a segurança dos novos medicamentos sofosbuvir, simeprevir e daclatasvir em pacientes portadores de arritmia cardíaca, particularmente em pacientes em tratamento com amiodarona ou digoxina.
Tratamento da hepatite C crônica
Não é o objetivo deste texto detalhar o tratamento da hepatite C, pois se tornaria demais cansativo e o protocolo está disponível a todos, conforme indicado na Referência no final do artigo.
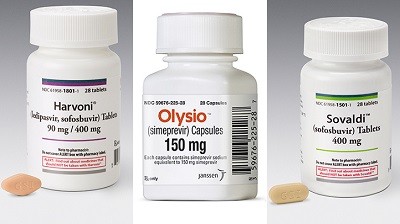
O Protocolo Clínico e Diretrizes Terapêuticas para Hepatite C e Coinfecções, 2015, do Ministério da Saúde incorporou novas drogas e o protocolo de 2018 ampliou as medicações disponíveis.
As novas opções apresentam outras vantagens, como facilidade posológica (são comprimidos), tratamento por menor período de tempo e com menos efeitos adversos, menor necessidade de exames de biologia molecular para avaliação do tratamento e melhores resultados.
Além de interferon peguilado e ribavirina, as medicações disponíveis para tratamento da hepatite C no Sistema Único de Saúde são:
- Daclatasvir (DCV) (inibidor do complexo enzimático NS5A);
- Simeprevir (SIM) (inibidor de protease NS3/4A);
- Sofosbuvir (SOF) (análogo de nucleotídeo que inibe a polimerase do HCV);
- Associação dos fármacos ombitasvir (3D) (inibidor do complexo enzimático NS5A), dasabuvir (inibidor não nucleosídico da polimerase NS5B), veruprevir (inibidor de protease NS3/4A) e ritonavir (potencializador farmacocinético);
- Associação de ledipasvir (LED) (inibidor do complexo enzimático NS5A) e sofosbuvir (SOF) (análogo de nucleotídeo que inibe a polimerase do HCV);
- Associação de elbasvir (EBR) (inibidor do complexo enzimático NS5A) e grazoprevir (GZR) (inibidor da protease NS3/4A).
Novos tratamentos em comprimidos
Muitas destas novas medicações apresentam diversas interações medicamentosas e o médico assistente definirá a medicação mais adequada e o melhor ajuste da dose e segurança.
Apesar da introdução de novos medicamentos, algumas modalidades de tratamento podem necessitar do uso de alfa-interferon peguilado ou de ribavirina.
Os esquemas terapêuticos variam de acordo com o genótipo e a história de tratamento prévio.
Eventos adversos (efeitos colaterais)
O tratamento com alfa-interferon peguilado e ribavirina para hepatite C é extremamente incômodo, pois determina diversas alterações laboratoriais e possíveis reações adversas que necessitam monitoramento clínico e laboratorial mais rigoroso.
Entre os principais eventos adversos do uso de alfa-interferon peguilado, destacam-se as alterações hematológicas (anemia, neutropenia e plaquetopenia) e sintomas que se assemelham aos da gripe (dor de cabeça, fadiga, febre e mialgia), além de sintomas psiquiátricos.
O uso de alfa-interferon peguilado também pode desencadear disfunção tireoidiana e dermatológica, além de doenças autoimunes.
Os novos medicamentos incorporados apresentam, como eventos adversos mais comumente reportados, sintomas comuns e leves. Podem ocorrer reações de fotossensibilidade e, por isso, recomenda-se ao paciente que evite exposição solar excessiva.
Alguns outros eventos adversos:
- com sofosbuvir:
- em associação com ribavirina: cefaleia e fadiga;
- em associação com alfa-interferon peguilado: insônia e anemia.
- com daclatasvir:
- em associação com alfa-interferon peguilado e ribavirina: rash cutâneo (manchas na pele), fotossensibilidade, coceira e náuseas.
Critérios para suspensão do tratamento
Conforme a Associação Americana para a Associação Americana para o Estudo da Doença Hepática e Sociedade de Doenças Infecciosas da América. o tratamento será suspenso nos seguintes casos:
- Ocorrência de eventos adversos importantes;
- Ausência de adesão ao tratamento;
- Identificação de situação que contraindique o tratamento, como a gestação;
- Elevação das aminotransferases em níveis 10 vezes acima do limite superior da normalidade;
- Infecção bacteriana grave, independentemente da contagem de granulócitos;
- Ocorrência de sepse;
- Descompensação hepática, como ascite e encefalopatia, significativo aumento de bilirrubina direta, em pacientes previamente compensados.
Monitoramento da eficácia terapêutica
Vírus HCV
A realização do teste para identificação do vírus por método de biologia molecular (HCV-RNA) está indicada para confirmar o diagnóstico de hepatite C crônica imediatamente antes de iniciar o tratamento, e na 12ª ou 24ª semana após o término do tratamento, para avaliar a eficácia terapêutica.
Reinfecção pelo vírus da hepatite C
É importante ficar claro que a hepatite C não confere imunidade protetora após a primeira infecção, havendo o risco de reinfecção.
Mesmo após a eliminação espontânea do HCV, na fase aguda ou após a RVS, o paciente permanece sujeito à reinfecção caso mantenha a exposição aos fatores relacionados à infecção.
Referências
- Ministério da Saúde (Brasil), Secretária de Vigilância em Saúde, Departamento de DST, Aids e Hepatites Virais. Protocolo clínico e diretrizes terapêuticas para hepatite viral C e coinfecções. Brasília (DF): Ministério da Saúde; 2018.

CRM-PR: 20322